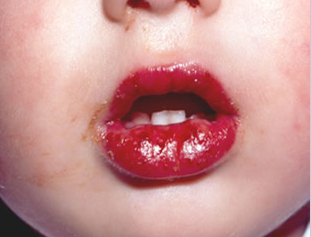
Doença de Kawasaki: A Revisão
Revisamos uma das vasculites mais comuns na infância, trazendo informações sobre a origem, o desenvolvimento e os tratamentos da Doença de Kawasaki.

Febre há 5 dias – esta queixa atendida nos prontos-socorros gera muita ansiedade por parte tanto da família quanto do médico, principalmente se algum diagnóstico ainda não foi estabelecido. Entre as inúmeras causas de febre mais prolongada, a doença de Kawasaki se destaca pois, se não for diagnosticada e tratada precocemente, o prognóstico do paciente pode ser severamente comprometido. Continue lendo a nossa revisão sobre o tema.
Introdução
A Doença de Kawasaki (DK) é uma das vasculites mais comuns na infância, e raramente ocorre nos adultos [1,2]. Antigamente era conhecida como síndrome do linfonodo mucocutâneo e foi descrita por Dr. Tomisaku Kawasaki em 1967 [3]. Ela frequentemente é autolimitada, com febre e manifestações inflamatórias agudas que duram em média 12 dias sem terapia.
A DK causa uma vasculite dos vasos de tamanho médio, com predileção pelas artérias coronárias, sendo causa frequente de doença cardíaca adquirida em países desenvolvidos [4]. A sua história natural e o tratamento são bem descritos, mas sua etiologia permanece obscura. Sua importância está no fato de poder ocasionar complicações graves, como por exemplo:
- aneurismas da artéria coronária,
- insuficiência cardíaca,
- infarto do miocárdio,
- arritmias e
- oclusão arterial periférica
Por conta disso, a DK pode levar a morbidade e mortalidade significativas, principalmente nos casos tratados inadequadamente [1,2 ].
Epidemiologia da doença de Kawasaki
Existe grande variabilidade de incidência de acordo com a geografia. A incidência em países subdesenvolvidos é desconhecida, dado o número escasso de trabalhos epidemiológicos. A população mais acometida são as crianças <5 anos (80%), embora a doença possa ocorrer até em adolescentes [. Apesar de ser incomum em <6 meses, ela responde por aproximadamente 10% das internações por DK nos Estados Unidos [2]
Os meninos são mais afetados que as meninas [2]. Em locais com prevalência elevada de sarampo, o diagnóstico pode ser difícil, devido à semelhança de sinais e de sintomas[2]. A partir dos anos 2.000, houve aumento da incidência da DK, mas este dados podem ser devidos somente ao maior conhecimento sobre a doença, o que permitiu a sua maior notificação. A incidência de DK é maior nas crianças do leste da Ásia ou naquelas que têm ascendência asiática e vivem em outras partes do mundo [2].
O país com maior incidência conhecida entre as crianças é o Japão, com 215 casos por 100.000, com incidência entre os meninos menores de 4 anos chegando a 240 por 100.000. Aproximadamente 1 em cada 100 crianças japonesas desenvolverão DK até os cinco anos de idade [2]. A prevalência no Japão é maior no inverno.
A incidência varia de acordo com país e ascendência [6]:
| LOCALIDADE | INCIDÊNCIA (EM 100.000 CRIANÇAS <5 ANOS) |
| Inglaterra | 8.39 |
| Austrália | 9.34 |
| Japão | 239 |
| Coréia do Sul | 134 |
| Taiwan | 66 |
| Havaí (descendência japonesa) | 210 |
| Havaí (sem descendência japonesa) | 13 |
Etiopatogenia
A etiologia da DK permanece desconhecida. Uma variedade de teorias foi proposta com base em dados patológicos, epidemiológicos e demográficos. Os dados epidemiológicos sugerem que uma infecção por um ou mais agentes que, geralmente, cursariam assintomáticos ou de forma não invasiva na maioria das crianças, em crianças geneticamente predispostas resultaria em DK [2]. Picos sazonais ocorreram nos Estados Unidos e no Japão, com maior incidência em áreas localizadas, sugerindo um vetor transmissível [6].
O consenso atual é de que provavelmente um gatilho (agente infeccioso) gere uma resposta imune anormal em pessoas com predisposição genética [6]. Até 2014, foram identificados 6 loci genéticos que estavam ligados à DK; entretanto, a etiologia da DK é complexa, e esses fatores genéticos ainda precisam ser totalmente aplicados ao diagnóstico e tratamento [7].
Resposta imune na DK
A resposta imune na DK acarreta uma inflamação sistêmica que afeta particularmente as artérias de tamanho médio, especialmente as artérias coronárias. Entretanto, múltiplos órgãos e tecidos podem ser envolvidos.
As sequelas a longo prazo parecem ocorrer apenas nas artérias. A lesão dos vasos sanguíneos resultam da infiltração de células inflamatórias nos tecidos vasculares, mas o estímulo para essa infiltração é desconhecido. A inflamação é mais intensa nas artérias coronárias e pode levar à destruição de células endoteliais luminais, da lâmina elástica e de células musculares lisas mediais. A dilatação e formação de aneurismas decorrem da destruição das fibras de elastina e colágeno e a perda da integridade estrutural da parede arterial. Participam do infiltrado responsável pela inflamação nas artérias coronárias:
- neutrófilos,
- células T (particularmente células T CD8),
- eosinófilos,
- plasmócitos (particularmente produtores de imunoglobulina A e/ou macrófagos, sendo esses últimos não participantes proeminentes em qualquer outro tipo de vasculite [2].
Origem infecciosa na doença de Kawasaki?
A suspeita de origem infecciosa é baseada em dados epidemiológicos que sugerem que a DK é causada ou desencadeada por um agente ou agentes transmissíveis. Alguns dados embasam este teoria[2]:
- A doença pode ocorrer em epidemias;
- A doença é rara em <6 meses; a transferência de anticorpos transplacentários poderia proteger essa faixa etária de alguns agentes infecciosos;
- O exantema febril com linfadenite e mucosite são características semelhantes a outras doenças infecciosas, como a infecção por adenovírus, sarampo e escarlatina.
- Aumento sazonal na incidência da doença no inverno e no verão em muitas áreas geográficas.
Ao longo dos anos, múltiplos agentes infecciosos foram associados ao desenvolvimento da DK, mas até o momento nenhum agente microbiano único surgiu como a causa predominante. Entre esses agentes destacam-se:
- Parvovírus B19,
- Neisseria meningitidis,
- Superantígenos mediados por toxina bacteriana,
- Mycoplasma pneumoniae,
- Klebsiella pneumoniae,
- Adenovírus,
- Citomegalovírus,
- Vírus Parainfluenza tipo 3,
- Rotavírus,
- Sarampo,
- Vírus de Epstein Barr,
- Vírus Linfotrópico Humano,
- Bactérias associadas a ácaros,
- Rickettsia e Propionibacterium acnes [7].
Manifestações Clínicas e Diagnóstico da doença de Kawasaki
A doença ocasiona febre, evidência de inflamação sistêmica e sinais de inflamação mucocutânea.
O diagnóstico é firmado pela história de febre de pelo menos 5 dias associada a 4 das 5 seguintes alterações:
- Conjuntivite bilateral não purulenta;
- Alteração da mucosa oral;
- Alteração de extremidades;
- Erupção polimórfica;
- Linfadenopatia cervical.
O diagnóstico baseado nesses critérios clínicos não tem 100% de sensibilidade e especificidade. Pelo menos 10% das crianças que desenvolvem aneurismas na artéria coronária não preenchem critérios para DK. Assim, as crianças que não atendem aos critérios podem ter uma forma incompleta de DK e devem seguir o algoritmo de DK incompleta [1] . Leia nossa revisão sobre Doença Kawasaki incompleta:
Doença de Kawasaki Incompleta – você sabe como diagnosticar?
Em publicação no Circulation em 2017, os critérios foram revisados e estão listados abaixo [8]:
| Febre ≥ 5 dias, sem outra causa definida, associada a 4 das 5 alterações: * se estiverem presentes 4 alterações, com febre de 4 dias, o diagnóstico também pode ser firmado |
| Hiperemia conjuntival bulbar bilateral sem exsudato |
| Alterações da mucosa oral: eritema e fissura labial, língua com aspecto de morango e / ou enantema da mucosa oral e faríngea |
| Alterações de extremidades: eritema e edema das mãos e pés na fase aguda e/ou descamação dos dedos com início na região periungueal na fase subaguda |
| Rash: maculopapular, eritrodemia difusa ou eritema multiforme-like |
| Linfadenopatia cervical (≥ 1,5 cm de diâmetro), geralmente unilateral |
Essas alterações, muitas vezes, não estão presentes aos mesmo tempo e não há regra na ordem de aparecimento. Assim, deve-se rever história e exames do paciente repetidamente, a fim de firmar diagnóstico nas crianças que ainda não fecham os critérios, assim como fazer o diagnóstico diferencial com outras possíveis doenças. Pacientes, geralmente mais velhos, com somente febre e linfadenopatia cervical inicialmente, tendem a ter um curso mais grave, com risco aumentado de doença da artéria coronária e falta de resposta à imunoglobulina [1].
Em relação à frequência de presença dos sinais e sintomas, o acometimento da mucosa oral é o mais prevalente, com 90%, seguido da erupção polimorfa em 70 a 90%, alterações nas extremidades em 50 a 85%, alterações oculares em> 75% e linfadenopatia cervical em 25% a 70% [1].
Manifestações

A conjuntivite caracteriza-se por eritema brilhante dos olhos e que, tipicamente, poupa o limbo devido à infiltração predominantemente bulbar. Em 70% das crianças com alterações oculares, a uveíte anterior pode se desenvolver. Portanto, o exame com lâmpada de fenda pode ser útil nos casos suspeitos. A presença de uveíte fornece mais evidências para o diagnóstico de DK, uma vez que é mais observada em DK do que em outras doenças com apresentações semelhantes [1].
As alterações da mucosa oral são: hiperemia e ou fissuras nos lábios, hiperemia difusa da orofaringe (enantema) e língua com aspecto de morango. Essas alterações podem ocorrer de forma muito leve e isoladamente. A presença de outros tipos de lesões orais, como vesículas ou úlceras e exsudato tonsilar, sugere outras doenças [1].
As manifestações cutâneas da DK são polimórficas. A erupção geralmente começa durante os primeiros dias da doença, tipicamente como eritema perineal e descamação, seguidos por lesões cutâneas maculares, morbiliformes ou em alvo, localizadas no tronco e nas extremidades. Lesões vesiculares ou bolhosas geralmente não são observadas. A DK pode desencadear uma erupção psoriasiforme em crianças não previamente reconhecidas como portadoras de psoríase [1].
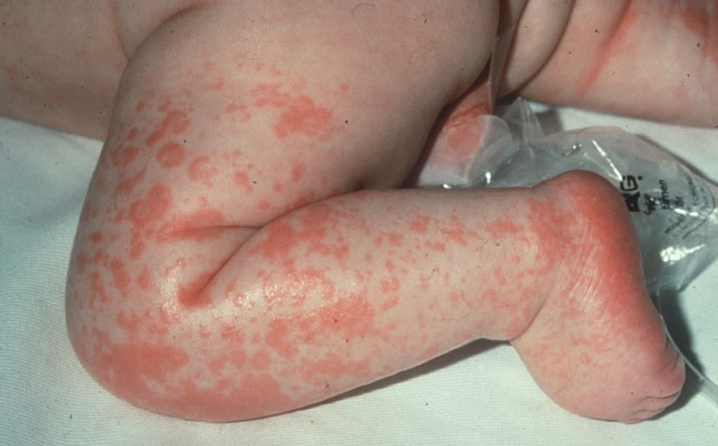
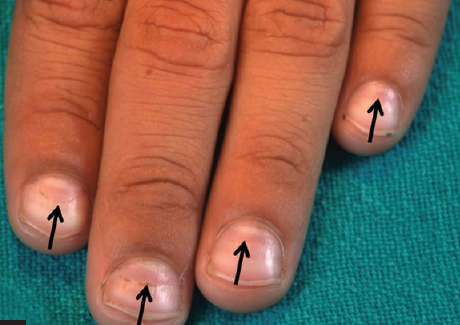
As alterações de extremidades geralmente desenvolvem-se tardiamente. No início, surge um edema endurecido no dorso das mãos e pés e um eritema difuso das palmas das mãos e plantas dos pés; posteriormente, há descamação em forma de folha, que começa na região periungueal das mãos e dos pés. A prevalência da descamação periungueal varia de 68 a 98%. Numa fase mais tardia, podem aparecer pregas transversais lineares nas unhas (linhas de Beau) [1].
A linfadenopatia cervical é a característica menos presente, podendo estar ausente em 50 a 75% dos casos. A linfadenopatia geralmente envolve os linfonodos cervicais anteriores; ao exame físico, freqüentemente apenas um único linfonodo grande é palpável, embora a ultrassonografia do pescoço demonstre numerosos nódulos distintos organizados em “cacho de uvas”. A presença de linfadenopatia difusa ou de outros sinais de envolvimento reticuloendotelial (esplenomegalia) sugere outros diagnósticos [1].
Os achados cardiovasculares não fazem parte dos critérios diagnósticos, mas auxiliam no reconhecimento, uma vez que a maioria dos diagnósticos diferenciais não acomete o coração. Nos primeiros 10 dias, podemos encontrar:
- taquicardia desproporcional à intensidade da febre,
- sons de galope e
- abafamento de bulhas.
Na ecocardiografia, aproximadamente 30% dos pacientes apresentam dilatação de uma artéria coronária no momento do diagnóstico. Os aneurismas não são vistos até o 10º dia da doença. Quadros graves, particularmente em crianças pequenas, podem apresentar aneurismas fusiformes das artérias braquiais, que são facilmente palpáveis ou visíveis nas axilas [1].
A artrite, apesar não fazer parte dos critérios diagnósticos, é autolimitada e não deformante, aparecendo em 7,5% a 25% dos pacientes. As grandes articulações são aos mais acometidas. Entre elas, destacam-se joelhos, tornozelos e quadril. Casos com acometimento articular geralmente cursam com níveis mais elevados dos marcadores inflamatórios (proteína C reativa ou velocidade de hemossedimentação) [1].
Outros achados inespecíficos podem estar presentes nos primeiros 10 dias antes do diagnóstico de DK:
- Diarreia, vômito ou dor abdominal (61%);
- Irritabilidade (50%);
- Vômitos (44%);
- Tosse ou coriza (35%);
- Perda de apetite (37%);
- Artralgia (15%) [1].
As três fases da Doença de Kawasaki
A doença de Kawasaki pode ser dividida em 3 fases: aguda, subaguda e convalescente. Alguns autores acrescentam uma quarta fase, chamada de crônica [7].
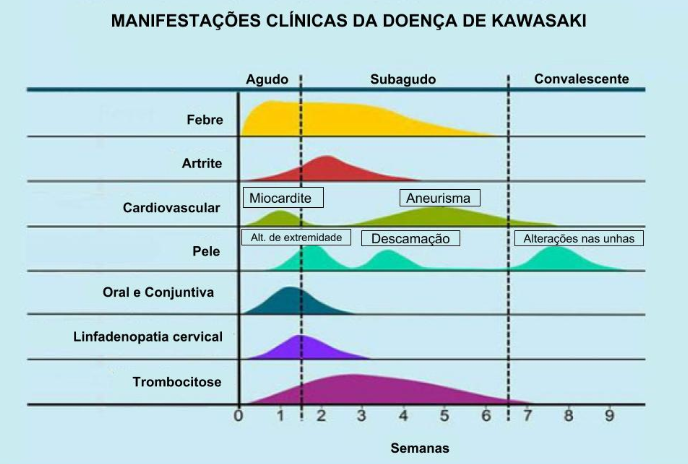
Na fase aguda, a febre é o principal achado. Ela tem início abrupto e dura geralmente 7-14 dias, podendo em alguns casos durar 3-4 semanas, quando não tratada. Após utilização da Imunoglobulina, geralmente remete em 36 horas. Além da febre, várias outras alterações podem ser encontradas, como: irritabilidade, meningite asséptica, otite média, uveíte anterior, miocardite/pericardite, pneumonite, disfunção hepática, renal ou gastrointestinal, orquite, vulvite (inflamação das pregas cutâneas da vulva), uretrite, eritema perineal e/ou descamação [7]. Pode haver, ainda, eritema, edema e formação de crosta no local de inoculação da vacina BCG, sendo este um achado que pode aumentar a suspeita da DK [1,6,7].

A fase subaguda inicia-se quando a febre diminui, e pode durar até 4-6 semanas. As características mais marcantes desta fase são: descamação dos dedos, trombocitose e o desenvolvimento de aneurisma da artéria coronária, aumentando assim o risco de morte súbita. Ocorre artralgia ou artrite com predileção para as grandes articulações de suporte de peso em 20-40% dos casos. Encontramos, também, hiperemia conjuntival, irritabilidade persistente e anorexia. Se houver persistência da febre por mais de 2-3 semanas, pode ser indicativo de reativação da DK, o que aumenta o risco de complicações cardíacas [7].
Na fase de convalescença, encontramos a resolução completa dos sinais clínicos da doença, o que ocorre, geralmente, dentro de 3 meses após seu início. Os reagentes de fase aguada e outras anormalidades laboratoriais retornam aos valores normais. Após 1-2 meses do início da febre, os pacientes podem apresentar sulcos transversais profundos nas unhas (linhas de Beau). Nessa fase, os aneurismas das artérias coronárias geralmente se resolvem por conta própria (60% dos casos), mas aneurismas maiores podem aumentar, assim como o risco de infarto do miocárdio. Em pacientes que tinham ecocardiograma previamente normal, a detecção de novos aneurismas é incomum após a 8ª semana da doença [7].
A fase crônica ocorre somente nos pacientes com complicações cardíacas. Os aneurismas formados na infância pode se romper na idade adulta [7].
Exames Laboratoriais


Está gostando desse texto?
Cadastre-se gratuitamente no PortalPed para ler o restante da matéria!